 BIOELEMENTOS, BIOMOLÉCULAS, AGUA Y SALES MINERALES
BIOELEMENTOS, BIOMOLÉCULAS, AGUA Y SALES MINERALES-Características de los seres vivos
La biología es la ciencia que estudia la vida. Los organismos son los que realizan las funciones vitales y la vida es una propiedad de la materia.
-Biología como ciencia
La biología abarca numerosos campos como la zoología y se ayuda de disciplinas como bioquímica. La biología es una ciencia empírica: observación, hipótesis, experimentación, análisis… Sus resultados deben darse a conocer. La biología ha abierto la puerta a técnicas muy variadas y potentes pero no están exentas de problemas éticos, jurídicos y económicos.
-Unidad química de los seres vivos
*Los seres vivos son diversos en apariencia, pero químicamente son muy similares.
*Materia viva=materia inerte.
*Selección química: la materia en el universo es básicamente H y He; en la corteza terrestre abundan O, Si, Al, Mg,… en los seres vivos los elementos principales son H y O, seguidos de C, N, S y P.
*La “elección” de elementos para la vida se basó en criterios de disponibilidad, comportamiento en medio acuoso y reactividad.
*Los bioelementos son 70 y forman biomoléculas. Según su abundancia, se clasifican en mayoritarios (primarios y secundarios), oligoelementos (esenciales y no esenciales).
*Las biomoléculas son sustancias por combinación de bioelementos (inorgánicas y orgánicas).
El C es un elemento similar al Si, pero más flexible en cuanto a las uniones que puede realizar y puede formar moléculas lineales o ramificadas, estables en condiciones terrestres, pero no como para reaccionar con otras. Puede unirse a numerosos elementos. El Si sólo forma cadenas lineales e inestables.
 -El agua
-El aguaEs “líquido de la vida”, tiene “propiedades extrañas”. Está formada por dos átomos de hidrógeno y uno de oxígeno, los orbitales del O forman un tetraedro, por otra parte, el O es muy electronegativo frente al H por eso el agua es neutra pero polar y es un dipolo. Forma enlaces de H. Las propiedades y funciones biológicas del agua son: acción disolvente (da lugar a tres tipos de disoluciones: moleculares, iónicas y coloidales; función vital: metabolismo y transporte de nutrientes y desechos), elevada fuerza de cohesión (F.V.: esqueleto hidrostático, turgencia y tensión superficial), elevada fuerza de adhesión (F.V.: capilaridad), gran calor específico (tampón térmico, homeotermia), elevado calor latente de evaporización (refrigeración por transpiración), menor densidad del hielo (F.V: superviencia) y otras como fotosíntesis e hidrólisis.
-Las sales minerales
Compuestos inorgánicos. Las sales insolubles: no se disuelven en agua, precipitan y forman estructuras sólidas, por lo que suelen tener función plástica (estructural) y actuar como protección y sostén. Las sales solubles se disuelven en agua y aparecen disociadas en iones (cationes y aniones), llamados electrolitos y realizan funciones catalíticas, funciones osmóticas, función tamponadora y nutrientes.
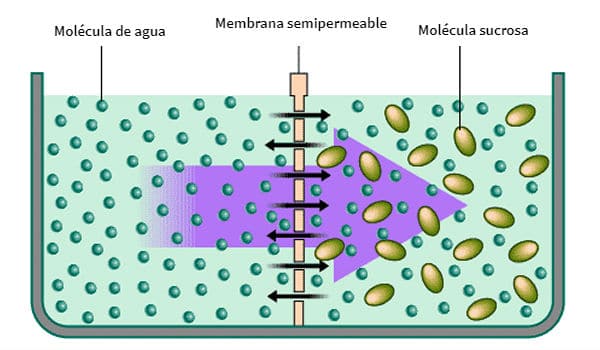
-Ósmosis y presión osmótica: La ósmosis es el paso de agua, a través de una membrana semipermeable, desde la disolución más diluida a la más concentrada. Presión osmótica sería la presión necesaria para impedir dicho flujo.Este proceso es importante en los seres vivos porque la membrana plasmática es semipermeable. Las disoluciones con igual concentración de solutos se denominan isotónicas. Una disolución es hipertónica si está más concentrada que otra (hipotónica) En células animales: en medio hipotónico entra agua, las células se hinchan (turgencia) y pueden estallar (lisis, hemólisis en eritrocitos); en medio hipertónico sale agua: deshidratación y muerte (crenación en eritrocitos). En células vegetales: en medio hipotónico entra agua y se produce la turgencia, pero la pared vegetal impide la lisis; en medio hipertónico sale agua, la membrana se separa de la pared y se rompe (plasmólisis), dando deshidratación y marchitez.
-Difusión y diálisis: Difusión: tiene lugar cuando dos disoluciones de diferente concentración están separadas por una membrana permeable o sin ella. Se produce el paso de solutos desde la disolución hipertónica a la hipotónica. Diálisis: permite separar solutos de pequeño tamaño de una disolución. Para ello se emplean membranas con poros de tamaño determinado.
GLÚCIDOS
-Conceptos de química orgánica
-Difusión y diálisis: Difusión: tiene lugar cuando dos disoluciones de diferente concentración están separadas por una membrana permeable o sin ella. Se produce el paso de solutos desde la disolución hipertónica a la hipotónica. Diálisis: permite separar solutos de pequeño tamaño de una disolución. Para ello se emplean membranas con poros de tamaño determinado.
GLÚCIDOS
-Conceptos de química orgánica
Es la química del carbono, el cual puede formar enlaces simples, dobles y triples. Los grupos funcionales son conjuntos de átomos que tienden a aparecer juntos en numerosas moléculas, tienen una nomenclatura y propiedades especiales y reaccionan en conjunto. Los más importantes son los hidrocarburos, los alcoholes, los aldehídos, las cetonas, los ácidos carboxílicos y las aminas.
-Hidratos de carbono
 El nombre deriva de su fórmula molecular (CH2O)n: El nombre es incorrecto, ya que al agua no aparece en la molécula. Los glúcidos se consideran como tales a los polihidroxialdehídos y polihidroxicetonas, sus derivados simples y los productos que forman entre sí o con otros mediante enlaces. Dada la enorme variedad de sustancias se dividen en osas y ósidos.
El nombre deriva de su fórmula molecular (CH2O)n: El nombre es incorrecto, ya que al agua no aparece en la molécula. Los glúcidos se consideran como tales a los polihidroxialdehídos y polihidroxicetonas, sus derivados simples y los productos que forman entre sí o con otros mediante enlaces. Dada la enorme variedad de sustancias se dividen en osas y ósidos.
-Osas o monosacáridos
Son polihidroxialdehídos o polihidroxicetonas de 3 a 9 átomos de C. La representación más sencilla se denomina proyección de Fisher.
-Derivados: No se ajustan a la fórmula general, ya que presentan otros grupos funcionales. Son los desoxiazúcares, los aminoazúcares y los ácidos urónicos.
-Propiedades: Físicas: sólidos, dulces, blancos, solubles, cristalinos, con isomería espacial y óptica. Químicas: el grupo carbonilo les da carácter reductor. Además, les permite enlaces hemiacetálicos internos, enlaces glucosídicos con otras moléculas y enlaces éster.
-Triosas: Los más sencillos, con 3 átomos de C. Existe sólo la dihidroxiacetona y el gliceraldehído (presenta un carbono asimétrico, es decir, con sus 4 valencias saturadas con radicales diferentes, debido a ello presenta isomería). Los isómeros son moléculas con la misma composición y estructura pero con diferentes propiedades. Existen muchos tipos de isomerías, las más importantes son: la Isomería espacial y la Isomería óptica.
-Triosas: Los más sencillos, con 3 átomos de C. Existe sólo la dihidroxiacetona y el gliceraldehído (presenta un carbono asimétrico, es decir, con sus 4 valencias saturadas con radicales diferentes, debido a ello presenta isomería). Los isómeros son moléculas con la misma composición y estructura pero con diferentes propiedades. Existen muchos tipos de isomerías, las más importantes son: la Isomería espacial y la Isomería óptica.
-Tetrosas: Monosacáridos con 4 C. Existen la eritrosa, la treosa y la eritrulosa (2 enantiómeros). Sin embargo, las aldosas tienen 4 isómeros. A las formas que se diferencian sólo en la posición del –OH del C asimétrico se les denomina D y L. El resto de estereoisómeros se diferencian por la posición del –OH en otros C asimétricos. Estos isómeros se denominan diasteroisómeros (siendo enantiómeros 2 a 2). Si la diferencia sólo se produce en un C asimétrico se llaman epímeros.
-Pentosas: Monosacáridos con 5 C. No se hallan libres, sino formando polisacáridos y otros compuestos. Destacan la ribosa y la desoxirribosa.
-Hexosas: Osas de 6 C. Las aldohexosas tienen 4 C asimétricos y las cetohexosas tienen 3. En la ciclación mediante proyección de Fisher en disolución presentan estructura ciclada en anillos. La ciclación se produce entre el C1 o C2 con el grupo hidroxilo del penúltimo carbono de la molécula, formándose un enlace hemiacetálico interno y el C1 o C2 se convierte en un C anomérico. La ciclación mediante proyección de Haworth permite que todos los enlaces tengan longitudes similares y permite ver los anillos en perspectiva. Se aprecia que el carbono anomérico da lugar a dos nuevos estereoisómeros (anómeros). Si el –OH queda hacia abajo se llama α y si queda hacia arriba, β. Las hexosas de interés biológico son la glucosa, la galactosa, la manosa y la fructosa.
Moléculas de 2 a 10 monosacáridos. Los más importantes son formados por la unión de 2 monosacáridos unidos por enlace O-glucosídico (puede ser dicarbonílico o monocarbonílico). Los principales son: la lactosa, la sacarosa, la celobiosa, la maltosa y la isomaltosa.
-Ósidos. Polisacáridos
Son macromoléculas por enlaces O-glucosídicos. Son los más abundantes y tienen funciones de reserva energética, estructural y reguladora. Son prácticamente insolubles, pero pueden retener y absorber agua. No son reductores.
-Homopolisacáridos: formados por la repetición de un único monosacárido. Lineales o ramificados. Pueden ser: pentosanas y hexosanas. También pueden ser celulosa, quitina, almidón (amilosa y amilopectina) y glucógeno.
-Heteropolisacáridos: formados por dos o más monosacáridos. Los más importantes son: hemicelulosas, pectinas, agar-agar, gomas, mucílagos, acido hialurónico, condroitina y heparina.
-Glucoconjugados
Compuestos formados por una parte glucídica unida a otra lipídica o proteica. Tienen funciones de sostén, protección y señalización en las membranas celulares.
LÍPIDOS
 Moléculas orgánicas formadas por C, O, H y, algunos, con S y P, insolubles en agua pero si en disolventes orgánicos. Son muy heterogéneos y según su estructura molecular pueden ser saponificables e insaponificables.
Moléculas orgánicas formadas por C, O, H y, algunos, con S y P, insolubles en agua pero si en disolventes orgánicos. Son muy heterogéneos y según su estructura molecular pueden ser saponificables e insaponificables.
-Ácidos grasos
Ácidos orgánicos con un grupo carboxilo unido a una larga cadena alifática. Son combustibles celulares, que pueden hallarse libres, pero suelen estar unidos mediante enlace éster a otras moléculas y se diferencian entre sí por la longitud de la cadena alifática y por el grado de saturación (saturados, insaturados o esenciales). Propiedades físicas: son moléculas anfipáticas, los saturados forman cadenas extendidas que se empaquetan fuertemente y presentan interacciones por puentes de H y por enlaces de Van der Waals, los insaturados, tienen curvaturas y su punto de fusión es menor: suelen ser líquidos a temperatura ambiente. Propiedades químicas: las insaturaciones facilitan la rotura de las moléculas, formando aldehídos volátiles de sabor y olor a rancio y son capaces de formar enlaces éster con alcoholes y otras moléculas, cuando se hidrolizan con álcali se forman sales de ácidos grasos (jabones), este proceso es la saponificación.
-Acilglicéridos
Ésteres de la glicerina o glicerol. Los más importantes son los triacilglicéridos (ésteres de la glicerina o glicerol con 3 ácidos grasos saturados o insaturados, iguales o diferentes). Las funciones de las grasas son reserva energética, servir de almohadilla protectora o aislante térmico y los animales presentan un tejido especial, el adiposo pardo o marrón. Las grasas se clasifican en sebos, mantecas y aceites.
-Ceras
LÍPIDOS
 Moléculas orgánicas formadas por C, O, H y, algunos, con S y P, insolubles en agua pero si en disolventes orgánicos. Son muy heterogéneos y según su estructura molecular pueden ser saponificables e insaponificables.
Moléculas orgánicas formadas por C, O, H y, algunos, con S y P, insolubles en agua pero si en disolventes orgánicos. Son muy heterogéneos y según su estructura molecular pueden ser saponificables e insaponificables.-Ácidos grasos
Ácidos orgánicos con un grupo carboxilo unido a una larga cadena alifática. Son combustibles celulares, que pueden hallarse libres, pero suelen estar unidos mediante enlace éster a otras moléculas y se diferencian entre sí por la longitud de la cadena alifática y por el grado de saturación (saturados, insaturados o esenciales). Propiedades físicas: son moléculas anfipáticas, los saturados forman cadenas extendidas que se empaquetan fuertemente y presentan interacciones por puentes de H y por enlaces de Van der Waals, los insaturados, tienen curvaturas y su punto de fusión es menor: suelen ser líquidos a temperatura ambiente. Propiedades químicas: las insaturaciones facilitan la rotura de las moléculas, formando aldehídos volátiles de sabor y olor a rancio y son capaces de formar enlaces éster con alcoholes y otras moléculas, cuando se hidrolizan con álcali se forman sales de ácidos grasos (jabones), este proceso es la saponificación.
-Acilglicéridos
Ésteres de la glicerina o glicerol. Los más importantes son los triacilglicéridos (ésteres de la glicerina o glicerol con 3 ácidos grasos saturados o insaturados, iguales o diferentes). Las funciones de las grasas son reserva energética, servir de almohadilla protectora o aislante térmico y los animales presentan un tejido especial, el adiposo pardo o marrón. Las grasas se clasifican en sebos, mantecas y aceites.
-Ceras
Mezclas complejas de lípidos apolares formados por la unión de un ácido graso de cadena larga y un alcohol también de cadena larga. Son muy apolares, sólidas e hidrófobas con función protectora y estructural. Se hallan en glándulas sebáceas de vertebrados, en cutícula de invertebrados, en hojas, frutos y tallos jóvenes, en la cera de abeja, en lanolina y en espermaceti.
-Lípidos complejos o de membrana
Formados por sustancias lipídicas y no lipídicas. Forman parte de las membranas biológicas, son anfipáticas.
-Glicerolípidos: Molécula de glicerina unida por enlace éster a dos ácidos grasos y a otra molécula que puede ser un monosacárido (gliceroglucolípido) o el ácido ortofosfórico (glicerofosfolípidos). Sus propiedades les permiten formar agregados (micelas, monocapas y bicapas)
-Esfingolípidos: Son derivados de la ceramida (ácido graso + esfingosina mediante enlace amida). Se clasifican en esfingoglucolípidos (ceramida + monosacárido mediante enlace O-glucosídico y pueden ser cerebrósidos si el monosacárido es simple o gangliósidos si el monosacárido es complejo con cadenas de oligosacáridos) y esfingofosfolípidos (ceramida + ácido ortofosfórico + etanolamina o colina mediante sendos enlaces éster y forman las esfingomielinas)
-Terpenos e isoprenoides
 Lípidos insaponificables derivados del isopreno. Se clasifican en monoterpenos, diterpenos, triterpenos, tetraterpenos y politerpenos.
Lípidos insaponificables derivados del isopreno. Se clasifican en monoterpenos, diterpenos, triterpenos, tetraterpenos y politerpenos.
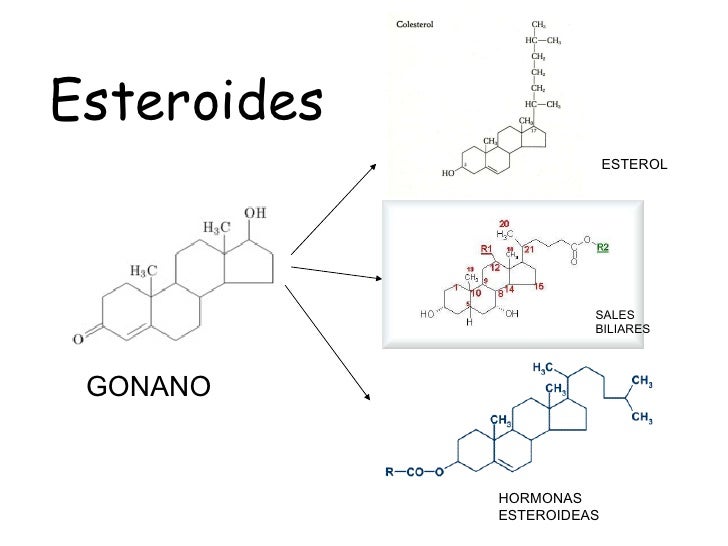
-Esteroides
Derivados del ciclopentanoperhidrofenantreno o gonano, que tiene cuatro anillos carbonados unidos. Se diferencian por los sustituyentes en el gonano y los dobles enlaces. Entre los principales están las sales biliares, los esteroles (grupo vitamina D y colesterol) y hormonas esteroideas (corteza suprarrenal, hormonas sexuales y ecdisonas).
-Eicosanoides
Moléculas derivadas de la oxidación de ácidos grasos esenciales. Actúan como mediadores en el sistema nervioso, el sistema inmune y la respuesta inflamatoria. Se clasifican en prostaglandinas, tromboxanos, leucotrienos y otros.
Fuente: BioGeo, Libro de 2º de Bach. de biología (Editorial Bruño), Moodle Biología 2º Bachillerato
Fuente: BioGeo, Libro de 2º de Bach. de biología (Editorial Bruño), Moodle Biología 2º Bachillerato

Comentarios
Publicar un comentario
Gracias por comentar. Te rogamos que seas preciso y educado en tus comentarios.